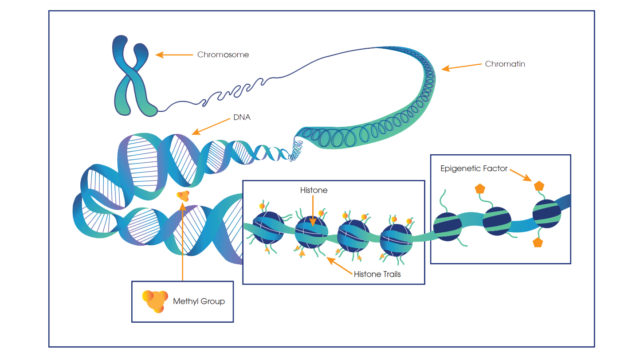
A petesejt (ovium) és a hím ivarsejt (spermium) találkozásakor történő megtermékenyítés alkalmával létrejött új egyed (nevezzük zigótának) génjei tartalmazzák mindazokat a lehetőségeket, amelyekre az új egyed képes lesz, de nem tartalmazzák az utasításokat, amelyek a gének megnyilvánulásához (génexpresszió) szükségesek. Ez az úgynevezett epigenetikai szabályozás keretében nyilvánul meg, tehát van egy gének feletti szabályozás, amely anélkül működik, hogy a DNS bázisainak sorrendje változna.
Adva van egy mechanizmus, amely a kapcsolótáblát – a gének által biztosított lehetőségeket – működteti. Csak az nyilvánulhat meg, ami az adott egyén génjeiben adott, de hogy mikor, mennyire és hogyan az a gének feletti (epigenetikai) szabályozástól függ. Adva vannak az egyedre jellemző gének, amelyek az egyed minden sejtjében egyaránt megtalálhatók és van az epigenom, amely minden sejttípusban más. A genom (a gének összessége) meghatározza például Kovács Józsefet, de nem határozza meg, hogy Kovács József melyik sejtje milyen funkciót lát el, más tehát Kovács József retinájának epigenomja, amely a látáshoz szükséges teendőket irányítja, mint májsejtjének epigenomja, amely a szerv emésztésben való részvételét határozza meg. Adva van tehát a kapcsolótábla és ennek elrendezettsége, amely egy bizonyos programra van beállítva a bázissorrend és az epigenom által, de a kapcsolások sorrendje és erőssége változtatható, egyes géneket ki is lehet kapcsolni, míg másokat lehet szomszéd vagy távoli gének működésétől függővé tenni, azaz átprogramozni a bekapcsolás sorrendjét, megerősíteni, vagy akár törölni, és ez történhet endogén módon, belső összefüggések hatására, vagy exogén módon, külső tényezők behatásának eredményeként továbbá külső és belső tényezők egymásra hatása miatt. Ezek jellemző rendszer-példája a fogváltás, amikor a tejfogak kihullanak és jön helyettük a maradandó fogak sora, vagy a menarche, az első menstruáció megjelenése és tartozékai, de ugyanígy a menopauza, az öregedés és jellemzői is. Ugyanígy benne lehetnek a programban kóros elváltozások, betegségek, amelyek adva vannak a génekben és csak megjelenésük ideje és erőssége változhat, de lehetnek a program megváltozásának eredményei is és ez mutatkozik meg betegségekként. Ugyanakkor, miközben az említettek rendszer szinten szólnak bele a programba, az epigenom határozza meg a mindennapi (genetikai) teendőket is, tehát hogy egy adott gén mikor kapcsolódjon be vagy ki, azaz mikor legyen parkolópályán és mikor működjék, tehát adjon utasítást egy fehérje (például enzim) termelésére, vagy annak leállítására. Mindennek összehangolt működése a normalitás (élettani működés) alapja. Ezt természetesnek vesszük és valóban az is, hiszen ennek működése alapján vagyunk képesek megítélni ember-mivoltunk, adott esetben normalitásunk (egészségi állapotunk) helyzetét és annak eltéréseit.
Az epigenomban metiltranszferázok és demetilázok működnek, tehát olyan enzimek, amelyek a DNS-re metilcsoportokat akasztanak, illetve távolítanak el. Mennél inkább metilált egy gén, annál kevésbé nyilvánul meg és mennél több metilcsoportot távolítanak el róla a demetilázok, annál inkább működőképes. Ez már önmagában is képes szabályozni a gének rövid, vagy hosszútávú megnyilvánulását, de ehhez még hozzájárul a DNS-t dajkáló hisztonok acetiláltsági foka éppúgy, mint bizonyos nem kódoló (mikro) RNS-ek tevékenysége is. Ez a rendszer alakítja ki és szabályozza a gének (bázissorrend) által biztosított programot, amely módosítható (átprogramozható). Az átprogramozással az adott gén helyzete, a rendszerben lévő többi génnel való kapcsolata, ezáltal tevékenységének ereje (expresszivitása) és minősége megváltozik. Miközben azonban az emberi gének bázissorrendjét már feltérképezték, az epigenom szerkezete és működése még nem tekinthető tisztázottnak ugyanakkor az elmondottakból is világos, hogy egy bonyolult és sokoldalú szabályozó rendszerről van szó.
Hibás hormonális imprinting és DOHaD
Az utóbbi időben számos vizsgálat mutatta ki illetve erősítette meg, hogy a terhesség harmadik harmadában (magzati vagy fetális korban) elszenvedett behatások (ártalmak) felnőtt korban megnyilvánuló betegségekhez vezetnek. Ezek között elsőként figyeltük meg még a múlt század nyolcvanas éveiben hormonok és hormonszerű anyagok receptor szintű károsító hatását, amelyet hibás hormonális imprintingnek neveztünk el [1][2].
A szervezet egészséges szabályozásához pontosan beállított endokrin (hormonális) rendszerre van szükség, amely a központi idegrendszer irányítása alatt, a szervezeti események gyors és összehangolt működését kontrollálja. Ehhez a tevékenységhez szükséges az endokrin (belső elválasztású) mirigyek rendszere, amely a hormonokat (jelmolekulákat) termeli és a receptorok rendszere, amelynek egyes, a sejtek külső membránjába épített, vagy sejten belül elhelyezkedő specifikus jelfogói ismerik fel és kötik meg a hormont, kiválasztva azt a
vérkeringésben vagy a szomszédságban levő molekulák tömegéből. Bár a szabályozás elvégzéséért legtöbbször a hormonokat teszik felelőssé, legalább ilyen, ha nem fontosabb szerepük van a receptoroknak, amelyek megléte nélkül a hormon hatástalan. A hormonális imprinting (beállítódás), amely perinatálisan (születés körül) történik meg, a receptorok fejlődésének illetve a receptor-hormon kapcsolatnak szükséges eleme, amely nélkül a receptor nem tud élethosszan normálisan működni. A receptor normális működése nélkül viszont a hormon nem tud hatni (üzenetet közvetíteni), így az adott hormonra vonatkozólag a belső elválasztású (endokrin) szabályozás hibás lesz. Még inkább hibás lesz azonban, ha a receptor beállítását nem a megfelelő hormon végzi el, hanem a receptorhoz az egyedfejlődés különleges állapotaiban (amikor az imprintáláshoz szükséges ablak nyitva van), kötődni képes molekula (a hormoncsalád egyéb tagja, szintetikus hormon, hormonszerű természetes vagy mesterséges anyag), azaz hibás imprinting lép fel. Ez, ha a magzati korban történik meg, funkcionális teratogenitásban (nem alaki, hanem funkcionális kóros fejlődésben, funkcionális torzulásban) nyilvánul meg. A korábban egyedüli teratogenitásként nyilvántartott (mert csak ennek felismeréséhez állt eszköz rendelkezésre) morfológiai (strukturális) teratogenitás (kóros fejlődés), már a magzat megszületésekor észrevehető volt, azonban a funkcionális teratogenitás rendszerint csak jóval később (betegségek formájában, vagy egyes funkciók hiányában) vehető észre [3][4]. A magzati korban provokált, de felnőtt korban manifesztálódó jelenséget nevezték el DOHaD-nak („developmental origins of health and disease” – egészség és betegség fejlődési eredete kezdőbetűi), ami azt jelenti, amit ennek a cikknek a címe is jelez: korai (fejlődési) ártalom késői (betegség, vagy egészség) következményekkel járhat és a „késői”, adott esetben évtizedeket jelenthet. Olyan betegségek, amelyeket korábban spontán fellépőknek tekintettünk, például schizophrenia (elmebetegség), autoimmun kórképek (amikor az immunrendszer az idegen helyett a sajátot pusztítja) szívműködési zavarok, elhízás, érelmeszesedés, stb. visszavezethetőkké váltak magzati kori ártalmakra, amelyeket korábban senki sem tartott kórokként számon és az összefüggések csak állatkísérletekkel (saját vizsgálatok), vagy emberek esetében matematikai-statisztikai módszerekkel (Barker vizsgálatai) váltak felismerhetővé és bizonyíthatóvá.
David Barker, a DOHaD teória kidolgozója belgyógyász és epidemiológus (járványtanász) volt és mindkét képzettsége, éppúgy, mint a (hibás) hormonális imprinting ismerete (amely ekkor már publikálva volt [1,2]) hozzásegíthette az elmélet kidolgozásához. Saját szakmai tapasztalatai azt mondhatták, hogy ha két orvosi (egészségügyi) esemény között statisztikai összefüggés mutatható ki, akkor ezeknek valóban közük van egymáshoz, és ebben az esetben ez fennállt: Angliában és Walesben a méhen belüli alultápláltság, csökkent újszülött kori testsúly és következményes fokozott újszülött kori halálozás statisztikai összefüggést mutatott a felnőttkori szív (koszorúér) betegek számával és elhalálozásával. Azaz kiugró értékek voltak megfigyelhetők évtizedekkel azután, hogy ugyancsak kiugró értékek voltak a vizsgált újszülött kori indexekben. A (hibás) hormonális imprinting koncepció arra hívhatta fel a figyelmét, hogy van lehetőség perinatális (születés körüli) ártalom memorizálására akár évtizedeken át, valamint felnőttkori hatásának látszólag spontán megjelenésére, így a két ismeretet összekapcsolva létrejöhetett a felnőttkori (nem fertőző, krónikus) betegségek méhen belüli traumával való magyarázata (ez a DOHaD teória [5][6]). Az első felismerést betegségek sorának (fejlődési eredetének) felismerése követte, amennyiben kimutatták a diabetes, elhízás, magas vérnyomás (esszenciális hipertónia), neuropszichiatriai kórképek, glukóz intolerancia, dislipidémia, rák stb. összefüggését egyedfejlődés alatti történésekkel. Ma már a 30 éves DOHaD koncepciónak nemzeti és nemzetközi tudományos társaságai, újságja, nemzetközi kongresszusai, tudományos díjai stb. vannak, mert alapvetően változtatta meg a nem-fertőző betegségek keletkezéséről alkotott képünket.
Mi történik?
Mint láttuk, minden egyed a genomja (a gének összessége) által meghatározott alapprogrammal jön a világra. A program működésében döntő szerepet játszik a gének DNS-ének metilációja. Mennél inkább metilált a DNS, annál kevésbé érvényesülnek az általa (gének által) hordozott információk. Mennél több metilcsoportot távolítanak el a demetiláz enzimek, annál több információ nyilvánul meg. A metiláltság leginkább (de több más tényező is, például hisztonok acetiláltsága, mikro-RNS-ek) szabályozza tehát a gének által hordozott információ megnyilvánulását, azaz a gének expresszivitását, a teljes gátoltságtól a teljes kifejeződésig. Az alapprogram lehet életre szóló, de belső és külső tényezők által változtatható. Az expresszivitás változása lehet átmeneti, de lehet tartós is, amely a következő átprogramozásig érvényes, vonatkozhat egyedi génekre és géncsoportokra illetve a teljes génállományra és hatásának mértéke ettől függően változó. Az alapprogramban a gének összehangoltan helyezkednek el, az átprogramozás ezt az egyensúlyt ideiglenesen vagy tartósan kibillenti, azaz megbontja azt a harmóniát, ami a szervezet normális működésének feltétele. A részleges átprogramozás ezért veszélyes, nem biztos ugyanis, hogy a megváltozott elemek anélkül illeszkednek vissza a rendszerbe, hogy kóros elváltozást (funkciózavar, krónikus betegség, rosszindulatú daganat) hoznának létre.
Programérzékenység
A beépített átprogramozásokon kívül, mint amilyen a már említett fogváltás, vagy az ivari tevékenységgel kapcsolatos események (pédául menarche és menopauza), durva hatásokra (például sugárhatás, mérgezések) bármikor történhet súlyos fokú átprogramozás. Vannak azonban időszakok, amikor az átprogramozás az adott szervezet igényei szerint történik, külső tényezők (például bizonyos molekulák) által. Ilyen időszak a perinatális periódus, tehát a terhesség 3. trimesztere, a közvetlen születés utáni periodus, az elválasztás időszaka, és kiemelkedően a kamaszkor. A kamaszkor (pubertás) a váltás időszaka, amikor teljes szervrendszerek, például az ivari apparátus, idegrendszer hatalmas mértékű átalakuláson mennek keresztül és ebbe az átalakulásba belefér nem-élettani tényezők általi átprogramozás is, életreszóló következményekkel. Olyan anyagok, amelyek egyébként (máskor) ártalmatlanok lennének, mindkét periódusban átalakítják a programot és hosszú távon, esetleg évek vagy évtizedek után megmutatkozó elváltozásokat hoznak létre. Ilyenek a már említett koszorúér betegségek, de a központi idegrendszer és immunrendszer betegségei is. A pontos mechanizmus nem ismert, de minden szervrendszernek vannak kritikus fejlődési peródusai, amikor az imprinting fogadására alkalmas ablak nyitva van. Ezen ablaknyitások többsége – mint már említésre került – a születés körül, azaz perinatálisan található, de pubertáskorban is megtörténik, miközben vannak minden szervrendszerben sejtcsoportok, amelyek ablaka nyitva van, bár maga a szerv már nem fogadóképes az imprintingre. Ugyanakkor éppen a teljesség hiánya, azaz csak egyes sejtcsoportok imprinting-érzékenysége vezethet el a betegség kialakulásához a harmónia megbomlása miatt, például rosszindulatú daganat-képződéshez. Extrém esetekben még öregkorban is lehetnek imprinting-váró sejtcsoportok idős szervekben (szervezetben), ami a kóros sejtátalakulás (daganat-képződés) alapja lehet, éppen az öreg szervezet fokozott védtelensége és az átalakult programú sejtcsoport agresszivitása miatt. Mindezt figyelembe véve a „kisded” fogalma szélesebb körű, mint annak általános értelmezése és a provokáció és megnyilvánulási időpont közötti különbségre inkább utal, mint a csecsemőkorra. Az imprintingre vonatkozó érzékenység tehát nem életkor-függő, hanem fejlődési állapot-függő, így lehet a valószínűsége nagyobb bizonyos életkorokban, amelyekre jellemző a sejtdifferenciálódás, de nem kizárt bármely életkorban, ha bizonyos sejtekben (sejtcsoportokban) éppen fejlődési (differenciálódási) folyamatok zajlanak.
Az ember immunitása elvileg két formában nyilvánul meg: a veleszületett (innate) és a szerzett (adaptív) immunitásban. Az innate immunitást mostanáig primitívebbnek tekintették, amely az általános immunitásért felelős, tehát ez áll az immunitás első vonalában, amely minden idegent ami a szervezetbe kerül, illetve ott válik idegenné elpusztitana, és csak mostanában lépett elő memóriával is rendelkező (trained) immunitássá, míg az adaptív immunitás (kezdettől fogva) felelősnek látszott az immun-memóráért, tehát azért, hogy amivel már korábban megküzdött, arra az újabb találkozáskor azonnal pusztítólag reagál (ez az oltások alapja). Lehetségesnek tűnik tehát, hogy a veleszületett immunitás felelős azért az immunitásért, amit eddig az adaptív immunitással nem tudtak megmagyarázni, például a DOHaD-ban szereplőért is.
A pubertáskort eddig is a káosz korszakának tartották, amikor korábban szokatlan és gyakran a későbbiekben eltűnő jelenségek jellemzők a kamaszra és ide beleillik a DOHaD fellángolása is, tehát újra a születés körüli időszakra jellemző módon jelenik meg az imprinterekre való érzékenység. Ez éppúgy tartós következményekkel jár, mint a perinatális imprinting. Ha tehát valakinél például 30-40 éves korában jelenik meg valamely nem-fertőző megbetegedés, az arra való hajlamot éppúgy beszerezhette már az anyaméhben, mint kamaszkorában. Egyesek éppen ezért az érzékenységi időszaknak a fogamzástól a pubertás végéig való kiterjesztése mellett kardoskodnak, ami nem valós, mert közben az érzékenység gyakorlatilag évekre szólóan nulláig csökken, csak újra megjelenik. A kamaszkor azonban nemcsak az imprinting létrejöttének kedvez, hanem a perinatálisan keletkezett hibás imprinting megnyilvánulásának is, mert ilyenkor nem működnek jól az elhárító mechanizmusok. A cikk címében is szereplő kisded tehát nem csak egy síró, vagy éppen mosolygós csecsemő lehet, hanem egy kellemetlenkedő kamasz, sőt nem tekinthető túlzásnak kijelenteni, hogy mindazok a sejtek (sejtcsoportok) lehetnek „kisdedek” amelyek megtartották fejlődési potenciájukat, így bármikor képesek akár rosszindulatú daganat provokálására is.
Provokátorok: teratogének és imprinterek
Minden trauma képes létrehozni hibás imprintinget, azaz átprogramozást, ugyanakkor a trauma minősége (fajtája, erőssége) befolyásolja a hibás imprinting tartamát és kiterjedését. Ebből a szempontból különösen lényeges a pszichés traumák figyelembe vétele. Míg egy fizikai traumatizáció hatástalan lehet a hibás imprinting kialakulása szempontjából, ha pszichés kapcsolatai nincsenek, a pszichés traumatizáció hosszútávú káros következményekkel járhat. Itt különösen kiemelendő a negatív pszichés stressz (diszstressz) hatása, a stressz-érzékeny periódusokban. A családi, éppúgy, mint a szociális környezet (óvoda, iskola) fontos szerepet játszhat a program tartós átalakításában és a késői időpontban manifesztálódó betegségek fellépésében, de a kritikus periódusokban megjelenő betegségek, legyenek ezek fertőzőek, vagy krónikusak, is lehetnek hosszú idő után megjelenő egyéb betegségek kiváltói, azáltal, hogy a trauma memorizálódik, majd – esetleg évtizedek múlva – következményei megjelennek spontán, vagy valamilyen provokáció hatására. Ebben jelentős szerepe van az immunrendszernek, amely sejtjeinek életkor-független differenciálódása miatt rendkívül érzékeny a hibás imprinterek fogadására és memorizálására, illetve a következmény (késői betegség) provokálására.
A humán evolúció évezredei alatt az emberi szervezet rengeteg imprinterrel találkozott, amelyek az immunrendszer működését befolyásolták, tartós hatást váltva ki annak élettani és kóros működésében. Ezen imprinterek többsége ma is megtalálható, mint testidegen környezeti kémiai anyagok: vulkán-kitörések és erdőtüzek valamint a dohányfüst termékei (dioxin, benzpirén), táplálkozási melléktermékek (fitoösztrogének: szteroid hormon jellegű és hatású molekulák, mint a szója genisteinje vagy daidzeinje; mikoösztrogének: gombák termelte szteroidok), amelyek valaha jelentős mértékben alakíthatták az emberi immunrendszert és működését, azonban korábban sohasem érhették el azt a mértéket, amely a modern ember mesterséges beavatkozása következtében létrejött. Ezek az „embercsinálta” anyagok, ahogy ma nevezzük őket: endokrin dizruptorok, hatalmas tömegben és variációkban zúdulnak az imprinting-érzékeny emberi szervezetre, amely közömbösítésükre nincs felkészülve, különösen a perinatális kritikus periódusban, amikor az elhárító rendszerek még kezdetleges állapotban vannak és hibás imprinting kialakulásával reagálnak a rohamra, azaz epigenetikailag átprogramozódnak, annak minden már említett következményével.
Az epigenetikusan létrejött változások át tudnak öröklődni az utódgenerációkra, így az általuk okozott probléma nem áll meg ott, ahol keletkezett. Nem tudjuk azonban hogy az öröklődés hány generációig tart. Emlősökben a 3. generációig kimutatható (nem vizsgálták tovább, mert hosszú a generációváltás). Feltételezhető azonban, hogy hosszabb nyomot hagy, az egysejtű modellben ugyanis 1000 generáció után is megmutatkozik a hatása. Ez azt jelzi, hogy evolúciós szempontból is problémák adódhatnak, bár még nem tudjuk melyek és mennyire súlyosak.
A zigóta méhen belüli fejlődése mesterségesen 3 periódusra osztható. Az egyedfejlődés elejére (embrionális szakasz), mikor a fejlődési potenciál kifejezett, és a sejtek osztódása gyors. Ez emberben a méhen belüli fejlődés első 3 hónapja, amikor a zigóta szerveinek alapstruktúrája és az egész szervezet vázlata kialakul. Ilyenkor a szervrendszerek és szervek érzékenysége külső behatásokra kifejezett és relatíve könnyen megzavarható, tehát létrejönnek a morfológiai (strukturális) rendellenességek, amelyek korábban a torzulások nevet viselték és amelyek már a születéskor felismerhetőek voltak, ugyanígy súlyosságuk fokozata is megbecsülhető volt. Már az ógörögök is észlelték a kóros elváltozásokat, amelyek viselőit csodalényeknek tartották, innen származik a kóros fejlődés tanának (teratológia) elnevezése (teras= csodalény, szörnyszülött), és a szülők dönthettek úgy, hogy a vének tanácsának engedélyével megszabadulnak a kóros utódtól, azaz kitehetik a Taigetos hegységbe, ahol a természeti erők és vadállatok elpusztítják őket, az emberi kegyetlenség eredményeként, vagy életben maradnak az emberi könyörületesség következtében (a gyermektelen párok, vagy jószívű emberek segítségével). A fogamzás utáni idő előrehaladtával a strukturális rendellenességek kialakulásának száma és intenzitása csökken, egyre inkább előtérbe kerülnek a funkcionális rendellenességek (amelyekről korábban nem is tudtak), és amelyek nem biztos, hogy kevésbé súlyosak, de biztosan kevésbé felismerhetők már a születéskor [7]. A vizsgáló módszerek fejlődésével napjainkra nőtt a felismert funkcionális teratogenitások gyakorisága, így az azokat okozó funkcionális teratogének száma is. Míg korábban főleg a terhesség első 3 hónapjában kellett figyelni a teratogénnek tartott molekulák elkerülésére, mert azt hitték, csak az ilyenkor provokált strukturális torzulások a kóros jelenségek, ma (a funkcionális teratogenitást is figyelembe véve) az egész terhesség alatt, sőt azon túl is.
Egyesek szerint a veszély-zóna a megtermékenyítéstől számítva 1000 napig tart, mások – többek között e cikk szerzője szerint is – bár fokozatosan csökken, serdülőkorban megint fellángol és születés körüli intenzitását éri el. Mindeközben – a morfológiai teratogénekkel ellentétben nő a funkcionális teratogének mennyisége és változatossága, amely a funkcionális fejlődési rendellenességek túlsúlyát hozza létre. Ezeket a rendellenességeket korábban nem is soroltuk a fejlődési rendellenességek közé, mert nem tudtuk, hogy fejlődési zavarokra vezethetők vissza, de ma már tudjuk, hogy azok, és következményeikben sem maradnak el a morfológiaiaktól: nem valószínű, hogy a hibás hormonális imprinting révén létrejött diabetest (ami funkcionális hiba) bármely orvos, vagy éppen maga a beteg a súlyossági sorrendben alább sorolná a kisujj egyetlen percének hiányánál (ami strukturális rendellenesség).
Morfológiai és funkcionális teratogének
A klasszikus (már az őskorban is feltűnő) fejlődési rendellenességek is jelentős mértékben eltértek egymástól: az anenkefáliát (agyatlanság) sohasem lehetett jelentőségében egy lapon említeni az agnathiával (az alsó állkapocs hiánya). Ugyanakkor mindkettő alapvetően különbözik például a diabetesztől, mert utóbbi mindezideig (belgyógyászati) betegségként lett besorolva, míg előbbiek a sors csapásaként. A diabetesz a kezelhető betegségek között szerepelt, míg az anenkefáliánál (mint a legtöbb morfológiai fejlődési rendelleneségnél, eltekintve sebészeti megoldásoktól a kisebb hibák esetén) ez szóba sem jöhetett. Miközben a morfológiai fejlődési rendellenességek voltak „az igaziak” aközben a funkcionálisak, ilyen formában meg sem jelentek, a szülők megnézték születéskor a gyereket (mint ahogy így tett az orvos, vagy a bába is és megállapították, hogy „megvan mindene” és az a fogalom, hogy valami még megjelenhet, amit a szülés időpontjában nem is keresnek (például egy daganat), vagy hiányozhat (egy betegség) fel sem merült. Bár korábban is felléphettek fertőző betegségek, ami a születéssel érkezett, az ott és akkor lezárult, most egyre több kóros állapot „van a batyuban” amik előbb vagy utóbb megjelenhetnek, az időzített bomba jelen van és bármikor fel is robbanhat. Ez önmagában nem okozna a korábbiaknál lényegesen nagyobb problémát, azelőtt is tudott volt, hogy bármikor produkálhat a gyermek olyan (például pszichés) problémát, amire korábban senki nem számított. A probléma a funkcionális teratogének felszaporodásával jár együtt, azzal, hogy megnőtt és folyamatosan növekszik előfordulásuk helye, mennyiségük és minőségük, miközben az emberiség növekvő igényei miatt felhasználási területük is (ipar, közlekedés, mezőgazdaság, gyógyszerek élelmiszerek), összefoglalva: míg korábban a (morfológiai) teratogén valami különleges volt (egy bizonyos gyógyszer, sugárhatás stb.), ma a (funkcionális) teratogén egészen mindennapi, fel sem tűnik [8]. Míg korábban a morfológiai teratogének felhasználási területe körülhatárolható volt, a funkcionális teratogének mindenhová bekerülnek, az ásványvizes palacktól a fogkrémes tubusig, a felvágott csomagolásától a növényvédő rovarölő szerekig. Míg korábban ki lehetett mondani, hogy a terhes nő kerülje el a sugárzó anyagokat a terhesség adott hónapjaiban, és meg lehetett határozni az időpontokat, ma sem az anyag, sem az időpont nem határozható meg pontosan, ha valaki egyáltalán élni akar, mert ma már a mesterséges anyagok nélkül az „élet” el sem képzelhető. Választanunk kell tehát, de nem egyedileg, hanem kollektíve, hogy azt a kemizált életmódot akarjuk folytatni, amit eddig szükségletünknek éreztünk, vagy visszavonulunk, amíg lehet, ha még lehet. Valószínűnek tűnik, hogy eddigi életmódunk is folytatható, csak azt nem tudni, meddig és hogyan. A morfológiai teratogének időszakában relatíve hamar megérkezett a válasz az életmódunk által megfogalmazott kérdésekre a már születéskor is észlelhető kóros jelenségek formájában, a funkcionális teratogének viszont lassan hívják elő a választ, lehet, hogy csak az élet vége felé, amikor már nincs is beavatkozási lehetőség. Nem vagyunk tisztában a funkcionális teratogének egymásra hatásának következményeivel éppúgy, mint a funkcionális és morfológiai teratogének egymásra hatásával. Ugyancsak nem vagyunk tisztában a dózisokkal, mi az a mennyiség, ami már létrehozza a fiziológiás, de nem hívja elő a hibás imprintinget, ugyanakkor – legalább is rövid távon – nem pusztítja el az embriót vagy a magzatot. És végül: nem vagyunk tisztában azzal, hogy mit is akarunk: azt hisszük lubickolunk a kellemes langyos vízben, pedig lehet, hogy ez a víz mérgezett. Azt sem tudjuk, a funkcionális teratogének mennyiben járultak hozzá immunrendszerünk fejlődéséhez és nem tudjuk megjósolni, mennyire teszik meg ezt a jövőben, ha újabb minőségeik és mennyiségeik jelennek meg, illetve, hogy ezt gátolni kell(ene) vagy épp ellenkezőleg elősegíteni, mert korábban hasonló jelenségekkel nem volt dolgunk, legalább is nincs róla tudomásunk, mert nem jegyezték fel a krónikák, amelyek éppúgy nem léteztek, mint maguk az inkriminált (ember-csinálta) anyagok.

Az emberiség történetét végig kísérték a fertőző betegségek (járványok), amelyek mennyisége és végzetessége napjainkra csökkent éppen az orvostudomány és (gyógyszer)vegyészet haladása következtében. Teljességében ugyan még nem sikerült a fertőző betegségeket felszámolni, de az arányok eltolódtak. Globális méretekben vizsgálva 2012-ben a halálozások 68 százaléka diabetesnek, ráknak, a keringési rendszer betegségeinek és krónikus tüdőbetegségeknek volt köszönhető, tehát olyan betegségeknek, amelyek fellépéséért nem bakteriális vagy egyéb fertőzések felelősek [9], de a korai fejlődési ártalmakra való visszavezetésük (DOHaD) jogosnak látszik. Egyelőre nem lehet kimondani, hogy kizárólagosan ennek köszönhető, de azt máris, hogy jelentős része, igen. Ez a tendencia nem látszik csökkenni, éppen ellenkezőleg: növekedőben van. Minden új kémiai anyag megjelenésével, tekintet nélkül annak ipari, mezőgazdasági, kommunális, táplálkozási, vagy egészségügyi felhasználására a funkcionális teratogenitás esélye nő. Ezek az anyagok egyre nagyobb mennyiségben, egyre többféle variációban, egyre inkább létszükségletként propagálva kerülnek alkalmazásra az elkényeztetett emberiség egyre szélesebb köreiben. Nem úgy, mint a baktériumok ellen, ezek ellen nincs gyógyszer, minden újonnan felismert vagy előállított gyógyszer csak a lehetséges funkcionális teratogének számát növeli, azokét az anyagokét, amelyek hosszú távon nem-fertőző betegségeket válthatnak ki. Fel lehetne tételezni, hogy ha már gyógyszer nem áll rendelkezésre, legalább elkerülésük csak hozzáállás, vagy rendeletek kérdése lenne, de a tapasztalatok nem ezt mutatják. Az emberiség szédületes mértékben növekvő létszáma és ezzel párhuzamosan igényeinek mind szélesebb körökben történő megjelenése mindezt nagyobb konfliktusok nélkül szinte lehetetlenné teszi.
A sérült kisded felbukkanása a felnőttben nem újkeletű jelenség, csak ennek felismerése az. A következmények leküzdésének módja azonban még várat magára. Vannak próbálkozások például a perinatális túltáplálás (és ennek következménye a gyermekkori és felnőttkori elhízás mint anyagcsere betegség) leküzdésére, de ezek még kezdetlegesek és népszerűtlenek, mert az emberiség sok évezredes fennállása alatt először kerül szembe tömegesen táplálékbőséggel a megszokott táplálékhiány helyett, és nem tudja elfogadni, hogy ez utóbbi is probléma lehet. Ráadásul a baktériumok és vírusok által terjesztett betegségek gyors megjelenésének megszokott ismeretében nehéz elfogadni az évtizedes (vagy akár fél évszázados) lappangási időket. Az egész mentalitásunkat át kellene állítani, de ez nem olyan egyszerű, márpedig e nélkül nem lehet bevezetni új szabályozást [10]. A jelek tehát nem biztatóak és az alagút vége még nem látszik. Ami azonban még kevésbé látszik: az alagút végén a fény.
CSABA GYÖRGY
IRODALOM
[1] Csaba G. Phylogeny and ontogeny of hormone receptors: The selection theory of receptor formation and hormonal imprinting. Biol Rev Camb Philos Soc 55, 47-63, 1980.
[2] Csaba G. The present state in the phylogeny and ontogeny of hormone receptors. Horm Metab Res 16, 329-335, 1984.
[3] Barker DJ, Osmond C. Infant mortality, childhood nutrition, and ischemic heart disease in England and Wales. Lancet 137, 1077-1081, 1986.
[4] Philips DI, Barker DJ, Osmond C. Infant feeding, fetal growth and adult thyroid function . Acta Endocrinol (Copenh). 129, 134-138, 1993.
[5] Barker DJP, Erikson JG, Forsén T, Osmond C. Fetal origins of adult disease: Strenght of effects and biological basis. Int J Epidemiol 31, 1235-1239, 2002.
[6] Charles M-A, Delpierre C, Bréant B. Developmental origin of health and adult diseases (DOHaD): Evolution of a concept over three decades. Med Sci (Paris). 32, 15-20, 2016.
[7] Csaba G.The faulty perinatal hormonal imprinting as functional teratogen. Curr Ped Rev 12, 222-229, 2016.
[8] Csaba G. A hormonális rendszer válsága: Az endokrin dizruptorok egészségügyi hatásai. Orv Hetil 158, 1443-1451, 2017.
[9] Brumana L, Arroyo, A., Schwalbe NR. et al. Maternal and child health services and an integrated, life-cycle approach to the prevention of non-communicable diseases. BMJ Glob Health 2, 2000295 2017.
[10] Csaba G. DOHaD (Barker hipotézis): egy betegségorientált, korszakalkotó, brit eredetű teória, magyar gyökerekkel. Orv Hetil 161, 16, 604-609, 2020.
A cikk a Természet Világa 2020. júliusi számában (151. évf. 7. sz.) jelent meg.