Tanulhatunk-e a molekuláktól?
A mesterséges fotoszintézis
megvalósításának lehetõségei
Ma már könyvtárakat lehetne megtölteni azokkal a cikkekkel, könyvekkel, amelyek azzal foglalkoznak, hogy milyen technikai megoldásokat alkalmaznak az élõlények érzékelésük, mozgásuk és általában az életmûködéseik során, és ezeket az ember hogyan használja fel különbözõ berendezések megtervezésében. Vagyis mit tanulhatunk mi az élõlényektõl?
Nem is gondolnánk, hogy az élõvilág legkülönfélébb szervezõdési szintjein, a szupraindividuálistól a molekulárisig találhatunk tanulnivalót. Érdemes az evolúció megoldásait is tanulmányozni, hiszen segíthet sok technikai feladat megoldásában.
Nézzünk erre egy érdekes példát! A vízbõl való lélegzésnek a légkörire való cseréje dramatikus változást okozott az oxigénszén-dioxid gázcsere hatékonyságában. Ezért a levegõbõl lélegzõ kétéltûek az oxigén felvételét fõképp a tüdõn keresztül, míg a szén-dioxid leadását inkább a nagyobb és nedves testfelszínen keresztül végzik. Mivel a bõrön keresztüli légzés a bõr elszarusodása miatt nehézkessé vált, egyre inkább a tüdõ vette át a szén-dioxid gázcsere elvégzésének a szerepét is. Ezt az egyre nagyobb felület lehetõvé is tette. Ugyanakkor kb. tízszeresére növekedett a szén-dioxid parciális nyomása a vérben (3-4 Hgmm-rõl 40 Hgmm-re), amit a szervezet a vér a HCO3-szintjének emelésével kompenzált. A kétéltûek légzése tehát (és a tüdõshalaké is, amelyek kopoltyúikkal inkább csak a szén-dioxid gázcserét végzik) kettõs mechanizmusú (bimodal) légzés. Most a kutatók azon fáradoznak, hogy bizonyos légzési elégtelenségben szenvedõ egyéneken ilyen bimodal mechanizmussal segítsenek (Nolte, 1998). Az oxigén felvétele megmaradna a tüdõ feladata, míg a vér szén-dioxid-mentesítése a testen kívüli berendezésben történne. Természetesen folynak kísérletek olyan berendezésekkel is, amelyek mind az oxigén, mind a szén-dioxid cseréjét elvégzik a testen kívül, sõt a testbe beépíthetõ változaton is dolgoznak (Vaslef és mtsai, 1994). Gondoljuk csak meg! Oxigénfelvétel és szén-dioxid-leadás! Vannak olyan élõlények, amelyek oxigént termelnek, és szén-dioxidot használnak fel életmûködéseik során a fotoszintetizáló szervezetek. Nem lehetne ezeket a szervezeteket (egysejtû algákat az egyszerûség kedvéért) rávenni arra, hogy ezt a vér számára is elvégezzék? Nos, folytatnak kísérleteket ilyen fotoszintetikus mesterséges tüdõ megalkotására is, de az az érzésünk, hogy ez ma még inkább csak érdekesség lehet, mint a közeljövõ sikeres gyakorlata (Basu-Dutt és mtsai, 1997).
Láttuk tehát, hogy az élõlényektõl
tanulva (innen indulva legalábbis) megalkothattuk a repülõgépet,
az ember a levegõbe emelkedhetett. Ma már bizonyára
megmosolyognánk azt, aki ezt szárnycsapásszerû
mozgásokkal szeretné elérni. Ám a természettõl
tanulva egyre tökéletesebb lehet az a berendezés is,
amellyel súlyos légzési nehézséggel
küszködõ embertársainkon tartósan segíteni
szeretnénk. Jó példái lehetnek annak, hogy
a szervezet, vagy a szervrendszer szintjén milyen hasznos dolgokat
leshetünk el az élõlényektõl életkörülményeink
javítására. A továbbiakban megkíséreljük
bemutatni, hogy mennyi hasznosat tanulhatunk a molekuláktól
egy mindannyiunkat nagyon-nagyon érintõ kérdés
megoldása érdekében.
A fotoszintetikus reakciócentrum
Vizsgáljuk például a fotoszintézist. Mivel a fotoszintetikus reakciócentrum szerkezetének és mûködésének a kutatása egymás után gyorsan két Nobel-díjat is kiérdemelt (Michel, Deisenhofer, Huber, 1988; Marcus, 1993), vegyük példának ezt a pigment-protein komplexet. Azért is, mert nyilvánvalóan e Nobel-díjaknak köszönhetõen (ugyanakkor a molekuláris biológia, az információ- és a számítástechnika fejlõdése miatt is) a molekuláris szerkezetkutatás legkedveltebb modellrendszere lett ez a molekularendszer. Ki gondolná, hogy mennyi hasznosat tanulhatunk ettõl a nem is olyan nagyon bonyolult molekulakomplextõl?
A fotoszintetikus reakciócentrum egy membránba orientáltan beágyazott pigmentprotein-komplex, amely képes az elnyelt fény energiáját stabil töltéspár energiájává alakítani. Ez a fehérjekomplex évmilliók óta a legtökéletesebben látja el ezt a feladatát, 100%-hoz közeli kvantumhatásfokkal, amit eddig egyetlen, ember által készített berendezés sem tudott megközelíteni. Mûködésének köszönhetjük nemcsak a mai oxidáló légkörünket, hanem azt is, hogy ki tudja meddig használhatjuk a bioszféra hajdan volt pozitív energiamérlegének tartalékait (a fosszilis energiahordozókat).
Régi vágya az emberiségnek, és egyre sürgetõbb
feladata is, hogy olyan berendezést készítsen, amelynek
segítségével tisztán, gazdaságosan,
megújíthatóan juthatunk energiához a lehetõ
leghosszabb (talán beláthatatlan) ideig. A megújuló
energiaforrások közül a szélenergia, az ár-apály
energia és a napfény energiája (napenergia) nyilvánvaló
lehetõségként vetõdik fel. A napenergia tûnik
a legalkalmasabbnak, egyrészt amiatt, hogy idõbeli és
térbeli eloszlása kiszámíthatóbb, ugyanakkor
tetemes mennyiségben áll rendelkezésre. Az a napenergia,
amely a Föld felszínére minden percben érkezik,
nagyobb, mint az egész emberiség éves energiafogyasztása.
Nem mindennapi kihívás tehát az, hogy ennek az energiamennyiségnek
akár a töredékét is hasznosíthassuk valamilyen
berendezésben. El kellene tehát képzelnünk valamilyen
berendezést, de milyen irányba is induljunk? Nézzük
talán meg egy természetben már mûködõ
napenergiát átalakító berendezés felépítését
és mûködését (például a fotoszintetikus
apparátust), és azt modellként felhasználva
próbáljunk meg felépíteni egy mesterségeset!
Nézzük meg, hogyan is mûködik az a berendezés,
amit a természet évmilliók óta olyan sikeresen
használ a napenergia megkötésére!
A fotoszintézis ahogyan õk csinálják
A fotoszintetikus reakciócentrum egy pigment-protein komplex, amelyben a fehérjevázhoz oxidációra ill. redukcióra képes pigmentek (kofaktorok) kapcsolódnak. A legjobban a baktériumok reakciócentrumát ismerjük. Ez ugyan nem képes oxigént termelni a vízbõl, de a foton energiáját képes stabil töltéspár energiájává alakítani, és a leglényegesebb tulajdonságaiban megegyezik a növények II. fotokémiai rendszerével. A fényelnyelés ebben a rendszerben is elektrongerjesztést jelent egy klorofill-típusú pigment (bakterioklorofill dimer, (BChl)2) amit primer donornak (D) is hívnak, p-elektronja magasabb, be nem töltött molekulapályára kerül. Az így keletkezõ nagy redukálóerõt képviselõ gerjesztett (BChl)2* rendszerrõl az elektron az egyre pozitívabb következõ kofaktorokra kerül úgy, hogy közben néhány átmeneti állapoton keresztül stabil töltéspár, elõször (BChl)2+/QA, majd (BChl)2+/QB alakul ki (1/a ábra). Itt a (BChl)2+ a közben oxidálódott primer donort, a QA és a QB pedig a redukálódott, kinontípusú elsõdleges illetve másodlagos akceptormolekulákat jelenti. Az elektronok mozgását az egyes komponensek redoxpotenciáljában meglevõ különbség irányítja úgy, hogy azok az egyre pozitívabb redoxpotenciálú rendszer felé haladnak. Ez egyben azt is jelenti, hogy a gerjesztés utáni töltésátmenetek során a szabadenergia-változás negatív, vagyis a töltéspár egyre inkább stabilizálódik.
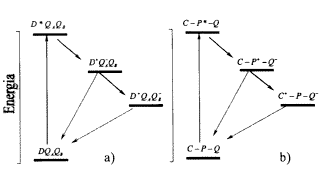
1.ábra. A fotoszintetikus reakciócentrum egyes kofaktorainak
(a) és a töltésstabilizálásra képes
"triád"-molekula (b) energiadiagramja. A két rendszerben
az energiaszintek abszolút értékükben különböznek,
az összehasonlítás tehát csak kvalitatív.
A folytonos vonal a töltésszétválasztást,
a pontozott vonal a töltésrekombinációs utakat
jelöli. A jelöléseket a szövegben értelmeztük
Fontos azt is észrevennünk, hogy ezek szerint az elektronáramlás nagyon határozottan egyirányú. Ezt az egyirányúságot alapvetõen a negatív szabadenergia-változás biztosítja. Elõfordulhat azonban bizonyos valószínûséggel az, hogy az elektron a töltésszétválasztás után visszajut a primer donorra (ezt a folyamatot töltésrekombinációnak nevezzük, amely nyilvánvalóan csökkenti a stabilizálódás hatékonyságát, hiszen újra (BChl)2QAQB, alapállapotú rendszert eredményez). Ennek a rekombinációnak a valószínûsége nagyon kicsi, különösen az in vivo rendszerben. Az élõ rendszerben ugyanis egy másodlagos donor nagyon gyorsan redukálja az oxidált primer donorunkat, még mielõtt az visszakapná az elektront a kinonmolekulától. Ezzel a folyamat gyakorlatilag egyirányúvá vált. Annak, hogy az oxidált primer donor gyorsan redukálódik, más, nagyon fontos jelentõsége is van. Az oxidált (BChl)2, a növényekben ennek megfelelõje a klorofill még inkább, rendkívül veszélyes a fehérjekörnyezetre. Annak lebomlását, degradálódását okozza. Másrészrõl a töltésrekombináció után a reakciócentrum-klorofillok a gerjesztett állapot egyik igen agresszív formájába kerülhetnének, ami ugyanígy veszélyes lenne a környezetre. Gyors redukciója tehát a töltésstabilizálódás hatékonyságának növelése mellett egy védelmi mechanizmus is egyben.
Az élõ szervezetben a reakciócentrum-komplexhez fénygyûjtõ antennarendszer is kapcsolódik. Ennek mûködését a mûholdvevõk parabolaantennájának a mûködéséhez hasonlíthatnánk a legjobban. Nélküle a parabola fókuszában levõ detektor ideje nagy részét csak azzal töltené, hogy várja egy hatékony rádiofotonnal való találkozását. A parabola a nagyobb felületén összegyûjti a rádiofotonokat, és a fókuszba koncentrálva juttatja a detektorhoz, megnövelve így az azzal való találkozás valószínûségét. A fotoszintetikus apparátusban is mûködik egy antennarendszer, ami az RC pigment-protein komplexhez továbbítja az összegyûjtött energiát. Ebben az antennarendszerben egyrészt több klorofillmolekula van, másrészt széles spektrumban elnyelõ karotinoidmolekulák, amelyek így kiszélesítik a hasznosítható spektrumtartományt.
Ez a rendszer tehát töltéspár energiájává (Coulomb- és redoxpotenciállá) alakítja a legtisztább energiaforrás, a napfény energiáját. Meg tudnánk-e valósítani azt, hogy a rendszer egyes komponenseit izoláljuk, ezek után összerakjuk úgy, hogy egy mesterséges membránrendszerben is mûködjön? Meg bizony! A fotoszintetikus apparátus bármelyik komponense, így az RC-komplex és a fénygyûjtõ LH-komplex (Light Harvesting) komplex is izolálható, tisztítható és a tisztított RC-komplex fény hatására töltésszétválasztást is végez. Sõt néhány komponensét már kristályos állapotban is elõállították (Deisenhofer és mtsai, 1984, McDermott és mtsai, 1995).
A töltéspár energiáját most már csak hasznos munka végzésére kell rávennünk!Ez azért nem olyan egyszerû. A fehérjét az evolúció olyan érzékeny berendezésnek alkotta meg, hogy az élõ szervezetbõl való kiszakítása után csak viszonylag rövid ideig õrzi meg stabilitását. Az igazat megvallva a növényi szervezetben is a második fotokémiai rendszer egyik fehérjéje (az ún. D1-protein) él a legrövidebb ideig, in vivo körülmények között is. Csak a növényi szervezet a lebomlott D1-proteint nagyon gyorsan újraszintetizálja. Ha meg is valósítanánk egy ilyen berendezést, feltehetõen nagyon gyakran kellene benne cserélni a fehérjetöltetet, hiszen igen valószínûtlen, hogy egy ilyen berendezéssel még fehérjét is szintetizáltathatnánk. Az meg egyszerûen elképzelhetetlen, hogy a berendezés maga szerelje össze az alkatrészeit (vagyis a pigment-protein komplexeit). A felhasználókat nagyon nehéz lenne meggyõzni arról, hogy vásároljanak egy energiaátalakító berendezést, amiben a leglényegesebb alkatrészt sûrûn kellene cserélni, ráadásul elég drága is lenne ez a csere. Más nehézségek is adódnak. A fehérjék izolálása, tisztítása hosszadalmas, nagy szakértelmet kíván, és nem is olyan olcsó dolog (fõképpen a több komplexbõl álló membránfehérjéké, mint pl. a fotoszintetikus reakciócentrumé, vagy fénygyûjtõ komplexé). Talán egy kicsit lehet optimalizálni, de nehezen képzelhetõ el drasztikus rövidítés mondjuk az idõ- vagy anyagigényen. A legfontosabb azonban az, hogy a reakciócentrumot az evolúció nem makro-, hanem nanoméretekre alkotta. Kisebb fényintenzitásokra, és kisebb teljesítményekre.
Akkor tehát adjuk fel a terveinket? Ne adjuk fel! Nagyon sokat
tanultunk a reakciócentrumtól! Hátha elõ tudnánk
állítani egy olyan mesterséges rendszert, amely nem
annyira érzékeny, mint a reakciócentrum, képes
a fény fotonjait elnyelni, és stabil töltéspárt
létrehozni.
Egy töltésszétválasztó mesterséges makromolekula
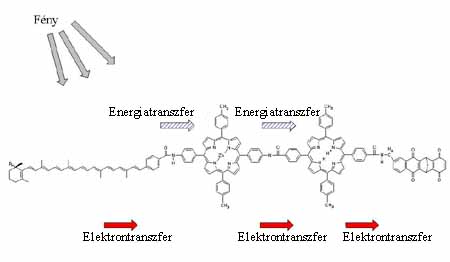
2. ábra. A töltésstabilizálásra
képes "triád"-molekula felépítése. Az
elektron- és töltéstranszfer irányát is
jelöltük
Keressünk egy olyan molekulát, amely széles spektrumtartományban képes fényt elnyelni ezek pl. lehetnek a karotinoidok. Majd egy olyat, ami ezt az energiát átveheti, és stabil gerjesztett állapotot hozhat létre. Ezt teszik a klorofillok a reakciócentrumban. A klorofilloktól pedig kinonmolekulák veszik át az elektront. Milyen érdekes lenne ezeket összehozni egyetlen molekulába. A 2. ábrán ilyen molekulát mutatunk be! Ha megnézzük ennek a molekulának az energiaszintrendszerét, akkor meglepõ dolgot tapasztalunk. Az 1/b ábrán a karotinoidokat C, a klorofill szerepét betöltõ porfirinegységet P, a kinont Q jelöli. Kísértetiesen hasonlít a fotoszintetikus reakciócentrum kofaktorainak energiaszint-rendszeréhez. És ami számunkra nagyon fontos, képes stabil C+-P-Q töltéspárt létrehozni (Steinberg-Yfrach és mtsai, 1997, 1998). Most már csak az a kérdés, hogy munkára tudnánk-e fogni ezt a rendszert? A kutatások eljutottak addig, hogy ez a triád molekula beültethetõ mesterséges lipidmembránba, hiszen van egy nagyon apoláros része, a karotinoid-molekula. A molekulának a lipidmembránba való beépülése sajnos nem irányított, hanem véletlenszerû, izotróp. Ez egy kis bonyodalmat okoz, hiszen mi azt szeretnénk, ha a töltésszétválasztás a membrán síkjára merõlegesen mindig azonos irányban történne. Van azonban valamilyen lehetõség az orientációra. Megfelelõ orientáció után, ha ehhez a lipid-molekulakomplex rendszerhez membránban oldékony kinonmolekulákat adunk, akkor ez a mozgékony kinon, mint a fotoszintetikus membránban is, képes elektronokat átvenni a triádhoz kötött redukált kinonmolekuláktól és átszállítani a membrán másik oldalára. Itt visszaadja az elektront az oxidált karotinoidnak, rövidre zárva ezzel a kört. De ez még nem minden! Ha a kinon két elektronnal redukálódik, kémiai tulajdonságaiból következõen ezt megteheti, akkor két protont is felvesz a vizes fázisból, és ezekkel együtt átdiffundál a membrán másik oldalára. Ott az oxidációja után leadja a két protont, szintén a vizes fázisba. Folyamatosan tehát egy protongradiens jöhet létre, aminek az elektrokémiai potenciálja munkára fogható. Legújabban sikerült ebbe a rendszerbe ATP1-áz fehérjekomplexet is beültetni, és ez a rendszer ATP-t szintetizált (Steinberg-Yfrach és mtsai, 1997, 1998).
Ez a példa nagyon jól igazolja, hogy létrehozható
egy olyan mesterséges rendszer, amely a természet által
jól kipróbált folyamatokat modellezi. Valószínû,
hogy nem ez az a rendszer, ami az emberiség energiagondjainak megoldásában
szóba kerülõ technikai lehetõségként
diadalmasan bevonul. Az viszont máris látszik, hogy az alapelvet
a kutatók felismerték, modellezni tudták, és
egy további, jól tanulmányozható rendszert
hoztak létre. Sõt, sikerült létrehozni egy olyan
összetett molekulát is, amely képes a hosszú
élettartamú, környezetére igen ártalmas
gerjesztett klorofillforma keletkezésének megakadályozására.
Ehhez egy másik, igen érdekes nagy molekulát, fullerént
kapcsoltak a porfirinvázhoz (Carbonera és mtsai, 1998), és
így egy védelmi mechanizmust is sikerült beépíteni
a molekulakomplexbe!
Félvezetõk alkalmazása
Ma már életünk természetes részévé váltak azok a berendezések, amelyekben a napfény energiáját valamilyen elmés szerkezet azok mûködtetésére alkalmas módon átalakítja. Ez a legtöbb esetben valamilyen fotoelektromos energiaátalakító berendezéssel történik. Bizonyára nem gondolunk a félvezetõk veztõképességének fizikai alapjaira, amikor mûködtetjük a zsebszámológépünket, fényképezõgépünket. Ilyen napelemek már nemcsak sapkákba beépített ventilátorokat, hanem autókat is mûködtetnek, de lakóházak, ûrállomások energiaellátását is megoldhatják. Sokféle félvezetõ alkalmazható, és ezzel a földfelszínre érkezõ napsugárzás spektrumához és az alkalmazandó berendezéshez a legjobban megfelelõt választhatjuk ki. Így például a titán-dioxid a látható spektrum legelején, a kék fényre, a kadmium-szulfid a zöld fényre (a földfelszínre érkezõ napsugárzás intenzitás-maximumához, kb. 560 nm-hez közel), a gallium-arzenid a távoli vörösre, az igen gyakran alkalmazott szilikon a közeli infravörösre érzékeny. Ezekben a berendezésekben a fény biztosítja azt az aktiválási energiát, amelynek hatására a vezetési sávba kerülhetnek elektronok. Több megoldandó feladat is felvetõdik, amelyek közül csak kettõt említünk itt. Sajnos ezeknek a celláknak a hatékonysága igen alacsony, 811% körül van, amit célszerû lenne növelni. Ehhez képest viszont igen drágák (néhány száz dollár négyzetméterenként).
Ott azért nem tartunk még, hogy a fotoszintetikus apparátus segítségével gyökeresen megnöveltük volna e berendezések mûködésének hatékonyságát, de az elmés kísérletekbõl sokat tanultunk már. Grätzel és munkatársainak sikerült olyan berendezést készítettünk, amely technikailag egyszerûbb, mint a hagyományos napelem, ezért olcsóbb az elõállítása is (Kay és Grätzel, 1993). Mûködésének alapja a fotoszintézis primer folyamatainak tanulmányozásából következett.
Megnövelhetjük egy napelem hatékonyságát, ha a fotoanódhoz kapcsolódó félvezetõ felszínére monomolekuláris festékréteget adszorbeáltatunk. A félvezetõ kristályok rendszerint keskeny sávban nyelik el a fényt, a gerjesztés diszkrét energiaszinteket érint. Hogyan lehetne szélesíteni a hasznosítható hullámhossztartományt? Olyan festéket kell választanunk, amely viszonylag széles spektrumban gerjeszthetõ, és képes a gerjesztett elektronokat a félvezetõ vezetési sávjának energiaszintjére emelni (3. ábra). Ezeket az alapokat már megtanultuk a fotoszintézistõl. Az is nyilvánvaló volt, hogy a klorofill az elsõk között volt a kipróbált festékek sorában, hiszen megfelel ezeknek a kívánalmaknak. Sajnos azonban igen labilis molekula, komoly árat fizet ezért a mûködéséért. Fény jelenlétében gyorsan degradálódik. Több festéket is kipróbáltak, és a legjobbnak egy szintetikus molekula bizonyult, amely stabil volt és abszorpciós sajátságai is megfelelõek voltak. (Ez a vegyület a cis(SCN)2-(4,4'-dikarboxi-2,2'-bipiridin)-ruthénium). Az abszorbeált foton a festék egy elektronját az elsõ legalacsonyabb be nem töltött molekulapályára emeli. Innen az elektron a TiO2 félvezetõ vezetési sávjába kerül, ahonnan a töltésrekombináció valószínûsége viszonylag kicsi. (Vagyis kicsi annak a valószínûsége, hogy az elektron visszakerüljön a festékmolekulára, mint ahogyan kicsi a fotoszintetikus elektrontranszport-láncban is.) Most már csak azt kell megoldanunk, hogy az oxidálódott festéket visszaredukáljuk, vagyis regeneráljuk, amit oldható redoxmediátor közbeiktatásával egy katódról megtehetünk. A katód és az anód közé fogyasztót kapcsolva, máris munkát végeztethetünk a rendszerrel. A megoldás nagyon elmés, jól felhasználja a fotoszintézis alapjairól szerzett ismereteinket. Sajnos a hatékonysága még kb. ugyanakkora, mint a hagyományos napelemeké, de árát figyelembe véve (ami alacsonyabb) biztató az alkalmazási lehetõsége.
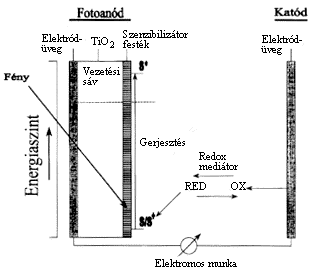
3. ábra. Egy félvezetõ napenergiacella vázlata. Az elektromos áram vezetésére alkalmas elektródüveg, a TiO2 félvezetõ és a szenzibilizátor festék együtt alkotja a fotoanódot. A katód szintén vezetõképes üveg. A RED és OX feliratok a redioxmediátor redukált és oxidált formáját jelölik
Antenna-cellák
Már volt szó arról, hogy fénygyûjtõ pigment-protein komplexek megnövelhetik a fényabszorpció valószínûségét, és kiszélesíthetik a hasznosítható spektrumtartományt. Ezekben a komplexekben a kromoforok közötti energiatranszfer olyan irányú, amely lehetõvé teszi a gerjesztési energia reakciócentrum felé történõ áramlását. Az egyes pigmentek abszorpciós tulajdonságai olyanok, hogy azok egy meghatározott energiagradienst hoznak létre a gerjesztés után. In vivo rendszerekben a reakciócentrum és az antennapigmentek között normális esetben nem történik elektronátadás. (Láttuk azonban, hogy a C-P-Q triádban a karotinoid-molekula elektront is átadhat a porfirinnek.) A legújabb krisztallográfiai vizsgálatok azt mutatták, hogy a fénygyûjtõ pigment-protein rendszerben a pigmentek elrendezõdése olyan, hogy biztosítja az elnyelt fényenergia komplexen belüli lehetõ leggyorsabb eloszlását, és a komplexek közötti energiagradiens menti transzportálását. Ezt egy igen nagyfokú szimmetriával tudja az élõ rendszer elérni. Elõ lehetne-e állítani egy olyan mesterséges antenna-rendszert, ami ilyen nagyfokú szimmetriával rendelkezik, nagy hatékonysággal abszorbeál fényt, és benne az energia egy központi energiacsapda felé koncentrálódva áramlik? Vannak biztató lépések! Wagner és munkatársai elõállítottak egy cinktartalmú tetra-aril-porfirin-származékot, ami egy központi porfirinhoz kapcsolódik etilénhidakkal (Wagner és mtsai, 1996). Ebben a rendszerben a Zn-porfirin szolgál fõképpen fényelnyelõ pigmentként, és az elnyelt fényenergia a központi porfirin felé áramlik. A rendszer kvantumhatásfoka nagyobb, mint 90%!! Miután a bíborbaktériumok fénygyûjtõ pigment-protein komplexének kristályszerkezete is ismertté vált (legalább is az egyik baktériumtörzs esetében), a kutatók olyan rendszerek létrehozását is elkezdték, amelyben porfirinszármazékokat kapcsoltak össze olyan szimmetrikus rendszerekké, mint ahogyan az az élõ szervezetben is van. Ezeknek a makromolekula-rendszereknek a vizsgálata még csak napjainkban kezdõdött, ezért korai lenne ujjongani, hogy megtaláltuk, amit kerestünk energiagondjaink megoldására.
***
A fotoszintetikus apparátus (itt a reakciócentrumot és a fénygyûjtõ komplexet tárgyaltuk) tehát sok mindenre megtanított bennünket. A tanulás folyamatos, egészen biztos, hogy sok tanulnivaló van még, de ma már tudjuk a következõket: olyan rendszert kell megalkotnunk, ami széles spektrumban nyeli el a fényt, képes energiatranszportot megvalósítani, vagyis energiavándorlás lehessen benne egy központi energiacsapda felé. Az elnyelt fotonenergiát stabil töltéspár létrehozására fordíthassuk, egyirányú elektrontranszportot tudjunk létrehozni. Növelhetjük a hatékonyságot, ha megvédjük a rendszerünket a fotooxidációtól.
Három lehetséges irányt mutattunk be arra vonatkozóan, hogy hogyan lehet a fotoszintézis primer folyamataiból, mondhatnánk azt is, a fotoszintézis makromolekuláitól tanulva a fotoelektromos, fotokémiai energiaátalakítást mesterséges rendszerekben megvalósítani. Mindegyik irány kísérleti stádiumban van még, bár láttuk, hogy különbözõ fejlettségi állapotokban. Talán a Grätzel-féle fotoelektromos cella az, ami a legjobban kidolgozott már, de drasztikusan valószínûleg nem fog változást elõidézni egyhamar az energiagazdálkodásunkban. A technológusok bizonyára sok kérdést fel tudnának tenni. A molekuláris biológus, biofizikus számára nagy kihívást jelentene egy olyan rendszer megalkotása, amelyben a reakciócentrum és a fénygyûjtõ komplex alapvetõ tulajdonságait együttesen tanulmányozhatná. Azt sem szabad elfelejtenünk, hogy ezekben a rendszerekben a kromoforok, redoxaktív kofaktorok, fehérjékhez kapcsolódva mûködnek. A fehérjék nemcsak egyszerûen a vázát adják a pigment-protein rendszereknek, hanem azokkal funkcionális egységet is alkotnak. Dinamikájukkal, térszerkezetüknek az elektrontranszporttal, energiatranszferrel együtt való megváltozásával modulálják az elektron- illetve energiatranszfer hatékonyságát, kinetikáját.
Lehet, hogy egyszer a kémikusok képesek lesznek megalkotni
olyan rendszert is, amely e faladatok ellátására is
alkalmas lesz?
A szerzõk köszönik az OTKA, OM FKFP, NATO és CNR támogatásait, amelyeket kutatásaikhoz, utazásaikhoz nyújtottak.
Irodalom
Balzini, V., Campagna, S., Denti, G., Juris, A., Serrani, S. and Venturi,
M. (1998) Acc. Chem. Res. 31, 2634
Basu-Dutt, S., Fandino, M. R., Salley, S. O., Thompson, I. M., Whittlesey,
G. C. and Klein, M. D. (1997) ASAIO J., 43, 279283
Carbonera, D., Di Valentin, M., Corvaja, C., Agostini, G., Giacometti,
G., Liddell, P. A., Kuciauskas, D., Moore, A. L., Moore, T. A. and Gust,
D. (1998) J. Am. Chem. Soc., 120, 43984405
Cogdell, R. J. and Lindsay, J. G. (1998) TIBTECH, 16, 521527
Deisenhofer, J., Epp, O., Miki, F., Huber, R. and Michel, H. (1984)
J. Mol. Biol. 180, 385398
Kay, A. and Grätzel, M. (1993) J. Phys. Chem., 97, 62726277
McDermott, G. et al. (1995) Nature, 374, 517521
Nolte, S. (1998) Anaesthesist, 38, 622625
Steinberg-Yfrach, G., Liddell, P. A., Hung, S-C., Moore, A. L., Gust,
D. and Moore, T. A. (1997) Nature, 385, 239241
Steinberg-Yfrach, G., Rigaud, J-L., Durantini, E. N., Moore, A. L.,
Gust, D. and Moore, T. A. (1998) Nature, 392, 479482
Vaslef, S. N., Cook, K. E., Leonard, R. J., Mockros, L. F. and Anderson,
R. W. (1994) ASAIO J., 40, M522526
Wagner, R. W., Johnson, T. E. and Lindsay, J. G. (1996) J. Am. Chem.
Soc., 118, 1118111193
US Department of Energy National Center for Photovoltaics, https://www.eren.doe.gov/pv/turning.html
Garab Gyõzõ: Kémiai Nobel-díj, 1988. A
fotoszintetikus reakciócentrum természete. Természet
Világa, 1998. évi 2. szám, 120. évf. 5355.
oldal
Aszódi Attila: Orvosi és kémiai Nobel-díjasok,
1993. Természet Világa 1994. évi 2. szám, 125.
évf. 5051. Oldal
Beck Mihály: Változatok
egy elemre. Kajtár Márton emlékének, ill.
Kémiai Nobel-díj 1996. Természet Világa 1996.
évi 11. szám, 127. évf. 482485. oldal
László István: A C-60 molekula megtalálásának
heurisztikai vizsgálata Természet Világa, 1998. évi
5. szám, 129. évf. 199201. oldal
Kiss Levente: Fullerén-szerkezetek
az élõvilágban. Természet Világa,
1998. évi 5. szám, 129. évf. 202. oldal