„A kémia számomra majdani képességek gomolygó felhője volt, mely tüzek fényétől szaggatott fekete oszlopaival beborította a jövőmet […]. Mint Mózes, attól a felhőtől vártam a törvényemet, a rendet, amely bennem lesz, meg körülöttem a világban.” – emlékezett vissza az olasz, vegyészből lett író, Primo Levi, hogyan tekintett a kémia tudományára gimnazista korában, a múlt század harmincas éveiben. A rendet, a megérthető és meg nem kerülhető természettörvények foglalatát várta tőle.
Az idézet születése óta eltelt nyolcvan-valahány évben valóban sokat fejlődött ez a tudomány, akkor előre nem látható mértékben gazdagodott nagyszerű eredményekkel, szélességben is, mélységben is. Éppen csak nem várjuk ma már tőle azt, hogy a természet megértésének ő adja a végső kulcsát. Levi dédunokája ma a fizikára, a biológiára, netán valamely modern területre, mint a biofizika, vagy a mesterséges intelligencia-kutatás nézne ilyen lelkesen.
Ez a folyó szétterült a természettudományok és a műszaki fejlődés nagyon sok vidékén. Eredményeit gyakran csak üggyel-bajjal lehet a diszciplína hagyományos keretei között elhelyezni. Persze ez az átalakulás nagyon régen megkezdődött. A magfizika atyját, az atommagot felfedező Rutherfordot 1908-ban kémiai Nobel-díjjal tüntették ki. Az ünnepséget követő banketten azt mondta: „Sokféle, különböző sebességű átalakulással foglalkoztam már, de ezek között a leggyorsabb az én átalakulásom volt, amikor egy pillanat alatt fizikusból vegyésszé váltam”. Az átalakulás valóban gyors volt, de azt hiszem, nem a tudós, hanem a tudomány alakult át ilyen sebesen.
A tizennyolcadik század közepén Lomonoszov már világosan megfogalmazta a fizikai kémia feladatát: „Ez a tudomány a fizika törvényei és kísérletei alapján megmagyarázza, hogy mi történik kémiai műveletek során az összetett testekben”. Szerényebben szólva, szeretné megmagyarázni. Mert gyakran nem megy a dolog. Néha a vegyész nem képes szabatos mérések alapján, helyes fogalmakat alkotva feltenni a kérdését. Máskor meg a fizika eszköztára nem elégséges még a válaszhoz. A kémia meglehetősen nagy tapasztalati anyagot gyűjtött össze a tizenkilencedig század közepéig. Ezeknek a felismeréseknek a szemléltetésére egyszerű modelleket alkottak, amelyeket nem csak elgondolni volt könnyű, hanem egy esztergályos műhelyében el is lehetett készíteni: itt az elemek atomjait kis golyók képviselik, belőlük épülnek föl a molekulák úgy, hogy a golyókat merev pálcikák, vagy hajlékony rugók kötik össze egymással. Gyermeteg elképzelés, szigorúbb gondolkodók, nagy tudósok, mint például Faraday, el is vetették ezt a „materialista asztalos munkát”. De ezek a naiv modellek, amelyek egyébként azóta is minden kémia tankönyvben szerepelnek, érthetővé-szemlélhetővé tettek (és tesznek ma is) egy sor kémiai megfigyelést. Azonban a golyókat összekötő pálcikák természetéről, vagyis a kémiai kötés tulajdonságairól hiába faggatta a vegyész Newton mechanikáját vagy Maxwell elektrodinamikáját, nem kapott kielégítő választ. A mostanában századik születésnapja felé közeledő, de még mindig modernnek tekintett kvantummechanika adta csak meg a helyes magyarázatot.
A kémia behatol az atommagba
Egy atom, tudjuk, pozitív magból és körülötte elhelyezkedő, negatív töltésű elektronokból áll. Két vagy több atom úgy alkot egy molekulát, hogy elektronjaik egy részét megosztják, azok többé vagy kevésbé egyszerre több atom környezetébe is települnek. Az atomok között megosztott elektronok: ezek tehát a golyókat összekötő pálcikák. Ez már szép, szabatos fizika, aminek az alapján a molekulák szerkezetét, a kötések energiáját is meg lehet érteni, sőt előre lehet látni. A kvantumkémia tudománya tárgyalja ezeket a matematikai szempontból nagyon nehéz kérdéseket. Ezen a területen új elméleti módszerek felfedezésével és a számítástechnika gyors fejlődésével nagyszerű eredményeket értek/érnek el a kutatók.
Az egyik alapvető feltételezés, amelyen az elmélet nyugszik, hogy a kémia eseményeit meghatározó elektronhéj nem befolyásolja az atommagok tulajdonságait. Hogyan is tehetné, hiszen a kémiai kötés vagy általában az elektronhéj energiája sok nagyságrenddel kisebb, mint a magban uralkodó, a magátalakulásokban szerepet játszó energiák. Aztán mégis!
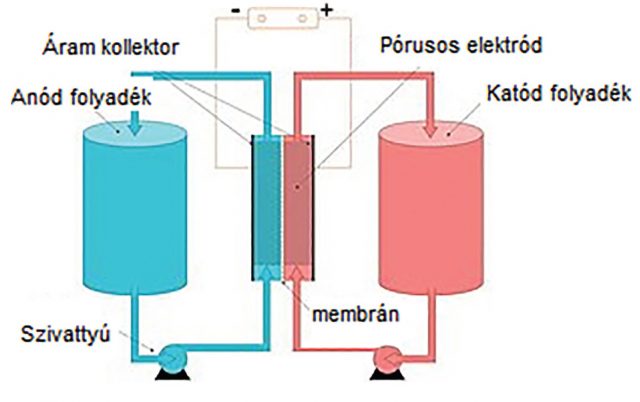
Az atommagok egy része, például a hidrogéné, amely mindössze egyetlen proton, mágneses térben úgy viselkedik, mint egy elemi mágnes. Állandó külső mágneses tér hatására igyekszik a tér irányába állni, ha még egy elektromágneses hullám is éri, úgy rezgésbe kezd. A rezgés frekvenciája attól is függ, hogy a rezgő atom szomszédságában milyen más atomok vannak. Más szóval az atommag rezgése a molekula szerkezetétől is függ. Ezen a jelenségen alapszik a mágneses magrezonancia módszere. Az 1. ábrán a metanol spektruma látható, amint feltárja, hogy kétféle állapotú H-atom van a molekulában. A módszer a kémiai szerkezetkutatásban is, vegyületek azonosításában is nagyon fontossá lett, de a beteg ember hétköznapjaiba is behatolt: ezen alapszik a nagyon elterjedt diagnosztikai eljárás, az MRI (mágneses rezonancia képalkotás) vizsgálat. Itt a szöveteink víztartalmának a segítségével tekintenek a testünkbe.
A mágneses magrezonancia az atommagok mozgását vizsgálja. Egy másik magfizikai eljárás, amely kémiai problémák megoldására is alkalmas, a radioaktív magok bomlását használja ki. Eléggé meglepő, hogy a héjelektronok energiájánál sok nagyságrenddel nagyobb energiákon végbemenő magfizikai átalalulások észreveszik, hogy milyen kémiai kötésben, atomi környezetben van az atommag. Pedig észreveszik, mert a mag energiaszintjei nagyon határozottak, igen csekély külső hatás is megváltoztatja őket. Éppen csak megmérni nehéz az ilyen kis változásokat, mert a radioaktív bomlás során a magból kilépő részecske meglöki a magot, ennek a mozgásnak az energiája pedig határozatlanná teszi az egyébként éles energiaszinteket. A Mössbauer spektroszkópia alapja az a felismerés, hogy ha a sugárzó atom egy kristályrács része, úgy a mérést nem zavarja a visszalökési energia, mert az eloszlik az egész kristályon. A 2. ábrán három, egymáshoz hasonló vastartalmú vegyület Mössbauer spektruma látható. Az eltérések szembeötlőek. Az eljárás nagyon sok vegyület szerkezetének a meghatározásán túl fontos a kohászatban, fémtechnológiában, kristálytanban, de a biológiában és az orvostudományban is: mindenütt számít a vegyületek összetétele, felépítése.

Méretek
A látható, tapintható testek mérete hatalmas a molekulákéhoz képest; egy köznapi értelemben vett kicsiny testben éppen úgy „végtelen sok” atom, molekula van, mint egy nagyban. Egy cseppentős üveg végén függő cseppet körülbelül 1019 vízmolekula épít fel. Ha azonban a méreteket tovább csökkentjük, meglepő jelenségekre bukkanunk. Kis méretű testeket kétféle úton állíthatunk elő, „föntről le” vagy „lentről fel”: vagy egy nagy testet aprítunk fel, vagy apró csírákat hozunk létre egy oldatban, olvadékban, esetleg gáztérben. Ez utóbbi eljárásokban a kémikusnak kell tevékenynek lennie. Egy apró csíra, pötty ugyan még nagyon sok atomból állhat, de a hosszmérete már elég kicsi ahhoz, hogy a benne lévő elektronok érezzék, falak közé vannak zárva. Fémek szulfidjaiból, foszfidjaiból elég könnyen lehet ilyen, úgy nevezett kvantum pöttyöket előállítani. Ezek közül sok anyag lumineszcenciára képes: ha rövidebb hullámhosszú fény éri, vagy elektromos feszültség alá helyezik, úgy meghatározott színű (hullámhosszú) fényt bocsát ki. Fénykibocsátó diódát (LED-et), napelemet, lézer diódát lehet belőlük készíteni, még az orvosi képalkotásban is szerepet kaphatnak.

Nem csak gömbölyű pötty, hanem vékony sík is viselkedhet meglepő módon. A 4. ábrán látható grafén a szénnek egy újabban felfedezett módosulata. Itt az atomok a síkban szabályos hatszögű rácsot alkotnak, a síkra merőlegesen azonban csupán egy atomnyi az anyag kiterjedése. Hiába hasonlít a rácsa a grafitéhoz, tulajdonságaik nagyon eltérőek. Ha alkalmas alakúra szabják, félvezetőként viselkedik, tehát tranzisztor, sőt integrált áramkör is építhető belőle. Legújabban pedig nagy kapacitású, gyorsan tölthető akkumulátorok anyagaként próbálják használni. Hasonló szerkezetű egyik rokona, a molibdén-szulfid, a szén-hidrogén ipar egyes folyamatainak hasznos katalizátora.

Energetika
Ennek a hatalmas területnek a fontosságáról nyilván nem itt kell írni. Ezen a helyen most csak néhány kérdésre telik. Egyfelől környezetkímélő, „zöld” üzemanyagokat szeretne mindenki használni. Ezeket az üzemanyagokat elő kell állítani. Másfelől egyre nagyobb területeken alkalmazzák a megújuló energiaforrásokat. A megújuló források pedig – itt főképp a Nap és a szél energiájára számítanak – az energia tárolását követelik meg, hiszen se a Nap nem süt állandóan, se a szél nem fúj mindig. Arról nem is beszélve, hogy a gyarló ember, méltatlanul feledve Darwin bölcsességét, egyre kevésbé szeretne alkalmazkodni holmi források szabta korlátokhoz. Energiát tárolni, egyéb módszerek mellett, elektromos energia formájában, akkumulátorokban lehet.
A környezetkímélő energiahordozók között természetesen a hidrogén áll az első helyen: vízből állítják elő és vízzé ég el, amikor felhasználják. Előállításához persze energia kell, és nyilván megkerüljük csak a problémát, ha fosszilis forrásokat égetünk el ebből a célból: ekkor nem az autó kipufogóján, hanem az erőmű kéményén száll el a szén-dioxid. Ha pedig a hidrogént metán és vízgőz közt lejátszódó, reformálásnak nevezett folyamat segítségével állítjuk elő, szén-monoxid is keletkezik. A víz elektrolízisénél ilyen gond nincsen, de az elektromos energiát valahonnan nyernünk kell. Oláh György azt írja, a nukleáris energia az egyetlen reális lehetőség. Így van-e?
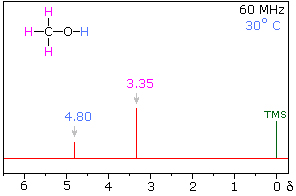
A tárolás dolgában, a régi ólom és az újabban elterjedt lítium akkumulátorok mellett mostanában sokat várnak a folyadék akkumulátorok régi gondolatától. Az 5. ábrán látható elrendezésben nem szilárd elektródok, hanem a két külön tartályban tartott anód- és katód folyadék tárolja az elektromos töltéseket. A keringő folyadékok között az áramkört egy olyan membrán zárja, amely csak a tárolásban szerepet játszó ionokat engedi át. Vajon ez lesz a megoldás? Akad még itt dolga a mai vegyészek unokáinak is.
SCHILLER RÓBERT
A cikk a Természet Világa 2019. augusztusi számában (150. évf. 8. sz.) jelent meg.