A szerves kémia, a tudományágak nagy többségéhez hasonlóan manapság az egyre összetettebb rendszerek vizsgálatát részesíti előnyben, miközben az egyszerűek is roppant nagy lehetőségeket tartogathatnak. A Debreceni Egyetem Alkalmazott Kémiai Tanszékét vezető Kéki Sándornak, és kollégájának, Nagy Miklósnak legalábbis, sikerült felfedezni egy olyan egyszerű molekulát, ami a rákgyógyászatban csakúgy szóba jöhet a fototoxikus gyógykezelés egyik elemeként, mint bizonyos környezetterhelések jelenlétének indikátoraként. A felfedezésről a két kutatót kérdeztük.
– Önök egy előadáson „svájci bicskaként” jellemezték molekulájukat. Hogyan értsük ezt a hasonlatot?
– A svájci bicska hasonlat a legutóbb előállított molekulánk, az izociano-amino-akridin (ICAAc) vizsgálata közben jutott eszünkbe, azért, mert egy molekulán belül négy vagy öt teljesen különálló alkalmazási területet tartalmaz, és szabadon megválaszthatjuk, hogy éppen melyiket kívánjuk – akárcsak a svájci bicska különféle eszközeit – „kinyitni”. A fenti hasonlat az általunk felfedezett alapmolekulára (ICAN) és származékaira egyaránt érvényes. Molekuláink előnyét az adja, hogy rendkívül egyszerű szerkezetük ellenére nagyon könnyen módosíthatók és a svájci bicska mintájára az alapszerkezet újabb és újabb funkciókkal bővíthető.
– Mitől függ, hogy mely tulajdonsága érvényesül éppen a molekulának?
– A vegyületcsaládot úgy kell elképzelni, mint egy aromás maghoz kapcsolódó izociano- és amino-csoportot. A tulajdonságok nagymértékben függnek egyrészt a szubszituensek pozíciójától, másrészt attól, hogy még milyen kiegészítő szubsztituensek találhatók az amino-csoporton: akár egy sima alkil-csoportról, vagy reaktív akril-csoportról beszélünk. Most abba az irányba mozdultunk el, hogy magát az aromás magot cseréljük le: az egyszerű naftalint akridinre, mert orvosi felhasználási lehetősége inkább az akridin származékoknak van.
– Azt mondják, hogy véletlenül fedezték fel a szóban forgó molekulát. Hogyan lehetséges ez?
– Évtizedek óta foglalkozunk polimerkémiával, azaz kis molekulákból polimerizációs reakcióval óriásmolekulákat állítunk elő. Egyik témánk során célul tűztük ki kék fényemittáló polimerek előállítását, amelyhez aromás izocianidokat (1-amino-5-izocianonaftalin, ICAN) választottunk kiindulási monomerként. Azért ebből a csoportból választottunk, mert az izocianidok reakciói rendkívül sokrétűek, nagyon sokféle átalakulásba vihetők. Amikor azonban elkezdtünk dolgozni az alapvegyülettel, rájöttünk, hogy nem kell feltétlenül polimerizálni, sőt, egyszerű molekulaként is borzasztó sokat tud.
Intelligens anyag, ami azt jelenti, hogy külső, környezeti ingerre szabályozott, előre kiszámítható választ ad. Szolvatokróm, vagyis különböző polaritású közegekben különböző színnel világít, lehetővé téve a molekula környezetének feltérképezését. Itt a környezeti hatás egy gerjesztő fény – ami általában UV fény – a kibocsátott fény pedig egy nagyobb hullámhosszú, vagyis kisebb energiájú fény, aminek a hullámhossza függ a közeg polaritásától. Előzetes vizsgálatok eredményei alapján nem ártalmas az élő szervezetre, így a későbbiekben orvosi felhasználása, például roncsolás mentes vizsgálatokhoz csakúgy szóba jöhet, mint ipari alkalmazása, például reaktor víztartalmának meghatározása felnyitás nélkül, vagy akár a higanyszennyezés természetes vizekben való jelenlétének kimutatásakor. Éppen ezért nagyon csodálkoztunk, hogy a szakirodalom tanúsága szerint eddig senki nem foglalkozott még ezzel az egyszerű molekulacsaláddal, mondhatni szűz területre tévedtünk. A miértre egy külföldi kolléga publikációnkat követő érdeklődése adta meg a választ. Ő ugyanis azt kérdezte tőlünk, hogy a molekulánk nem büdös-e?

– És nem az?
– A miénk nem, de „rokonsága” alapján joggal tételeznénk fel róla, hogy büdös. Az alifás, tehát telített szénhidrogénekhez kapcsolódó izocianidoknak rendkívül kellemetlen szaga van, túlzás nélkül állíthatjuk, hogy kegyetlenül büdösek. Lieke az 1850-es években írta le, hogy ha egy üvegnyi allil-izocianidot kinyitunk egy szobában, három napra emberi tartózkodásra alkalmatlanná válik az adott helyiség. Ez olyannyira nem tréfa, hogy egyes hadseregek/rendvédelmi szervek gondolkodtak már nem halálos vegyi fegyverként történő alkalmazásukban is, például tömegoszlatáskor. Ezt azonban akkor, amikor polimer kutatásainkhoz monomernek választottuk, mi még nem tudtuk. Ha tudtuk volna, valószínűleg mi sem nyúlunk ehhez a vegyületcsaládhoz. De nem tudtuk, így hát megcsináltuk.
– Említette, hogy roncsolásmentes vizsgálatokhoz alkalmazható lehet a molekula. Használható lehet élő emberi sejt vizsgálata során is?
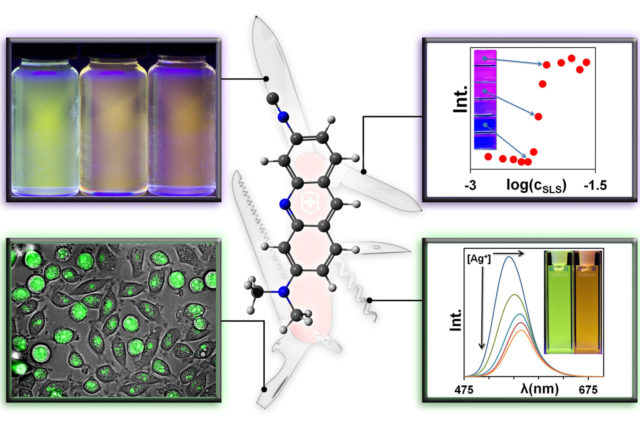
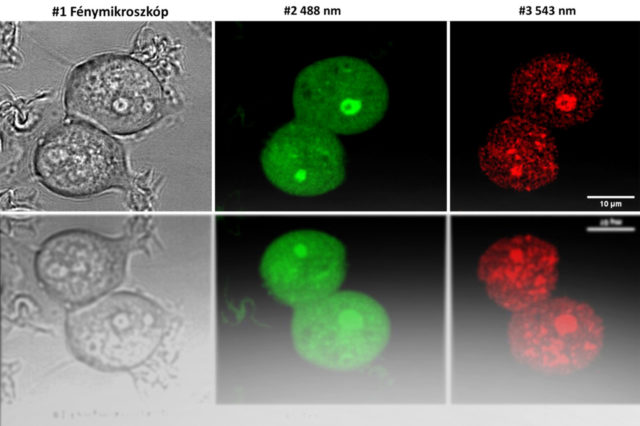
– Már általános- vagy középiskolában végzett mikroszkópos bemutatókon megtanulja az ember, hogy a legtöbb sejt maga átlátszó, mivel nagyrészt vízből áll. Egyszerű fénymikroszkóp alatt, kis túlzással, csak a sejtfal és a sejtmag látszik, semmi egyéb. Bármely sejt viszont több millió vegyületből áll, és ahhoz, hogy tudjuk, ezek hogyan és hol rendeződnek el, valamilyen módon meg kell festeni őket. Ennek két fajtája van a vitális, és a nem vitális festékek. A nem vitális megöli az élő sejtet, így értelemszerűen csak preparátumnál használható. Vitális festéknél ezzel szemben élve maradnak a sejtek, tehát dinamikus folyamatok is követhetők. Ez egy-egy betegség kialakulásánál rendkívül fontos, mert például ráknál is a felgyorsult anyagcsere miatt oxigénszegény környezet alakul ki, és a hypoxia következtében a közeg savasabb lesz. Ha tehát egy olyan molekulát tudunk előállítani – egyébként, a Scientific Reports-ban ezt publikáltuk – ami savas közegben dúsul, akkor a rákos sejtekben megnő a koncentrációja, ami lehetőséget teremt a fototoxicitáson alapuló rákgyógyászatra. De egy ilyen festék alkalmas lehet a rákos sejt felfedezésére is. Mivel ez a vegyületcsalád, amivel dolgozunk, nagyon könnyen szubsztituálható az amino-csoporton, akril-amino-izociano-naftalint állítottunk elő, amit ACAIN-nak neveztünk el. A vegyület érdekessége, hogy az akrilát észtercsoport miatt úgynevezett fluoreszcencia kioltás jelenség lép fel, és az észter csoport eltávolítása után az ACAIN visszanyeri a fluoreszcenciáját. Az ACAIN ezen tulajdonsága azért lehet izgalmas a rákdiagnosztikában, mert a rákos sejtekben, főleg emlőrák esetében, az észteráz enzimek aktivitása a tumorsejtekben emelkedett. Molekulánkat a Növénytani Tanszéken már vizsgálták, és ott kimutatták, hogy növényi sejtekben vitális festékként használható. Meg kell említenünk továbbá, hogy ma Magyarországon ritka az olyan felfedezés, amikor egy, az egyetemen előállított originális anyagot az egyetem többi tanszékének kutatói saját kutatásaikhoz használjanak, interdiszciplináris kutatócsoportokat létrehozva. Molekuláink iránt nagy érdeklődés tapasztalható az orvosok és a biológusok részéről, eredményeinket már több közös nemzetközi közleményben is ismertettük. Most távlati célunk az, hogy bevisszük a rákos sejtbe, és a kifényesedést tanulmányozva módszert dolgozhatunk ki a nagy észteráz aktivitás kimutatására, vagyis a rák jelenlétének jelzésére.
– A diagnosztikán túlmenően van-e egyéb gyógyászati alkalmazási lehetőség ebben a vegyületcsaládban?
– A rákterápiás módszerek közül az úgynevezett fototoxicitás, amihez olyan világító molekula kell, ami rákos sejtben jobban dúsul, mint a környező sejtekben. Mivel ennek gerjesztéséhez a normál sugárterápiás eljárásokban alkalmazott gamma-sugárzásnál jóval kisebb energiájú UV-fény kell, alkalmazása sokkal előnyösebb lehet. A környező szöveteket nem károsítja, viszont fény hatására gyökös folyamatok játszódnak le a tumorsejtben, oxigéngyök képződik, ami szétveri azt. Vagyis, ha csak a rákos sejtben van az előzőekben már említett akridin származék (ICAAc) egyszerűen azért, mert csak ott dúsul, akkor csak ott képződik az oxigéngyök, és csak azt veri szét a környező szövet sérülése nélkül.
– Az akrilcsoportot hordozó izociano-amino-naftalin (ACAIN) egy véletlen felfedezés volt: az alapmolekulát polimerizálni akarták a kettős kötésen keresztül, és akkor vették észre, hogy az akrilcsoport bevitele teljesen más fotofizikai tulajdonságokat eredményez. Ennek alapján indultak el abba az irányba, hogy megpróbálják felfedezésüket a biológiai jelölésre hasznosítani. Nem lehet ezt fordítva csinálni, vagyis hosszadalmas, több ezer kísérlet elvégzése helyett a szerkezetből kiindulni?
– A fotofizikai tulajdonságok és a szerkezet között nagyon nehéz összefüggéseket találni. A szuperszámítógépek elterjedésével és a kvantumkémia fejlődésével lehet ezeket számolgatni, de csupán a szerkezet alapján nem tudja megmondani az ember, hogy ez most biztosan világítani fog-e, vagy esetleg egy rejtett effektus miatt kioltódás játszódik le. A kioltódás nemcsak belső hatás eredménye lehet, hanem okozhatja a festékmolekula közelébe kerülő más molekularészlet vagy ion is. A piridin, ami egy kis molekulájú vegyület, és elterjedt oldószer a kémiában ilyen fluoreszcencia kioltás jelenséget mutat például naftil-aminoknál, amelyet a fluoreszcencia spektroszkópia nagyjai, például Mataga is vizsgált. Harminc évvel ezelőtti méréseik során, a 2-amino-naftalin vizsgálatánál egy olyan csökkenő görbét kaptak, ahol a piridin-koncentráció növelésével a fluoreszcencia pár százalékhoz tendált, de nem ment le nullába. Nem tudtak elfogadható magyarázatot adni a jelenségre. Az ICAN származékok piridines kioltódás vizsgálata során nagy meglepetésünkre a fluoreszcencia először majdnem nullára csökkent kis mennyiségű piridin hatására, majd tiszta piridinben ismét nőtt és elérte az eredeti érték 20 százalékát. Ilyen jelenséget eddig nem írtak le a szakirodalomban. Hosszas mérések és kvantumkémiai modellezés után arra jutottunk, hogy nem csak gerjesztett állapotbeli komplexképződés történik piridinnel, ami kioltja a fluoreszcenciát, hanem alapállapotban is jelen van egy úgynevezett ICAN-piridin pi-komplex, ahol a két aromás gyűrű síkja párhuzamos egymással. E komplex mennyisége a piridin-koncentrációval emelkedik, és ha létrejött újabb piridin, már nem képes kioltani a fluoreszcenciát. Bár e komplexek képződését a 2000-es évek elején számolásos úton már megjósolták, tudomásunk szerint mi voltunk az elsők, akik kísérletileg is kimutatták, és ezzel egy közel 30 éves rejtély oldódott meg.
A sikeres gyakorlati alkalmazáshoz a fent említett elméleti nehézségek miatt több száz vegyületet kell előállítani, és megnézni, hogy ezek közül melyiknek legjobbak a fluoreszcens tulajdonságai. Nekünk az a mázlink, hogy rögtön belenyúltunk a legjobba, az 1,5-ICAN telitalálatnak bizonyult. Bármelyik másik szubsztitúciós pozíció sokkal rosszabb fotofizikai tulajdonságokkal bír, ahogyan azt egy mostanában megjelent publikációban részletezzük. Pedig az egyik leghíresebb szolvatokróm festék, a Prodan analógiájára azt hittük, hogy a 2,6 pozíció jobb lesz, mert minél messzebb van a két csoport (amino és izociano) egymástól, annál hosszabb a gerjesztési tengely, és annál jobb tulajdonságainak kellene lenni, de a gyakorlatban ez nem így van.
– A molekulák egyike a higanyt is kimutatja. Milyen környezetanalitikai felhasználása lehet ennek a tulajdonságnak?
– Egyes jelentések szerint évente öt-nyolcezer tonna higany kerül a levegőbe – de olyan is van, aki azt mondja, hogy akár húszezer tonna is lehet ez a mennyiség – elsősorban a széntüzelésű erőművek füstgázából. Ez bekerül utána a talajba, vizekbe, élővilágba, táplálékláncba, és végül az emberben köt ki, tehát ezért nagyon fontos bárhol a higanynak a kimutatása, a mi kis egyszerű molekulánkkal pedig ezt terepen is meg lehet csinálni. Nem kell bonyolult műszert vinni, hanem kivisszük az ICAN-nak elnevezett molekulánkat, vagy valamelyik származékát, belecseppentjük a vízbe, és egy egyszerű fotométer – vagy akár egy UV-lámpa segítségével is megmondható, hogy van-e higany, legalább is higany(II)-ion a vízben, vagy nincs. A távlati cél pedig az lenne, hogy mivel a higany(II)-ion só formában oldódik vízben, az elemi higany pedig nem, szeretnénk egy olyan vízszűrő-berendezést csinálni belőle, mondjuk egy szivacsot, amin ha a higannyal szennyezett vizet átengedjük, akkor visszaredukálja a higany(II)-őt higannyá. A kinyert higany olcsó szelektív módszerrel összegyűjthető egy kád alján. Lehetséges így a szelektív higanykivonás mondjuk szennyvíz iszapból, bányaiszapból, és a kivont fémet esetleg újra tudjuk hasznosítani.
– Mi az a többlet, amitől az ICAN jobb lehet higany kimutatásában, mint a jelenleg alkalmazott más anyagok?
– Mai tudásunk szerint az ICAN a legkisebb molekulatömegű festék, ami higany fluoreszcens meghatározására használható, és emellett a higannyal egy időben képes az ezüst kimutatására is. Ez pedig azon alapul, hogy az ezüst komplexet képez az izonitril-csoporttal, a higany viszont, reakcióba lép vele, és visszaalakítja aminná. Ez a kettősség az izocianid- csoportnak köszönhető. Így érhető el, hogy egy ennyire egyszerű vegyület ennyire különleges és eddig még le nem írt tulajdonságokat mutasson.
DOMBI MARGIT
A cikk a Természet Világa 2020. márciusi számában (151. évf. 3. sz.) jelent meg.





